“BNT162b2-elicited neutralization of B.1.617 and other SARS-CoV-2 variants”
J Liu, YLiu, H Xia, J Zou, S C. Weaver, KA. Swanson, Cai, et al.; University of Texas
Nature (2021); Received: 19 May 2021; Accepted: 4 June 2021; Published online: 10 June 2021
https://www.nature.com/articles/s41586-021-03693-y_reference.pdf
El síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2) continúa evolucionando en todo el mundo, generando nuevas variantes que son preocupantes en función de su potencial para alterar la transmisibilidad, patogenicidad y cobertura de vacunas y terapias.
Estas mutaciones pueden promover la unión del pico al ACE2 o reducir la capacidad de neutralización, pudiendo alterar la transmisión del SARS-CoV-2, el tropismo tisular y el resultado de la enfermedad.
Destaca actualmente una segunda ola masiva de COVID-19 en la India, que se ha asociado con la expansión de las variantes B.1.617.1 a 32 países, B.1.617.2 a 49 países y B.1.618 a 6 países. La variante B.1.617.2 (delta) ha mostrado evidencia de transmisibilidad particularmente alta en el Reino Unido.
Otra variante, B.1.525, detectada inicialmente en Nigeria, se ha extendido a 49 países.
Por este motivo, la OMS ha designado el linaje B.1.617 (India) como variante motivo de preocupación y al B.1.525 (Nigeria) como variante de interés.
La vacuna BNT162b2 (BioNTech & Pfizer), es una vacuna basada en RNAm, con una eficacia del 95% contra COVID-19 y que ha sido autorizada por la FDA en Estados Unidos para la vacunación de personas mayores de 12 años.
La finalidad del estudio ha sido analizar la efectividad de neutralización provocada por la vacuna Pfizer BNT162b2 frente a estas variantes emergentes.
Para comparar la susceptibilidad de neutralización de las diferentes variantes, se realizó una prueba de neutralización de reducción de placa al 50% (PRNT50) usando un panel con 20 sueros recogidos de sujetos humanos inmunizados con la vacuna Pfizer, que se extrajeron 2-4 semanas después de dos inmunizaciones con la vacuna, espaciadas con tres semanas de diferencia.
Se ha analizado en estos 20 sueros humanos la neutralización del SARS-CoV-2 diseñado a partir de una cepa de virus aislada en enero de 2020 (USA-WA1/2020) y de virus quiméricos de glicoproteínas de pico correspondientes a las variantes B.1.617.1, B.1.617.2, B.1.618 (todos identificados por primera vez en India) y B.1.525 (identificada por primera vez en Nigeria).
Cada suero se probó simultáneamente para su PRNT50 contra el virus WT y mutantes.
Los títulos de neutralización contra los virus variantes, en particular la variante B.1.617.1, parecen más bajos que el título contra el virus USA-WA1 / 2020, pero todos los sueros analizados neutralizan los virus variantes en títulos de al menos 40.
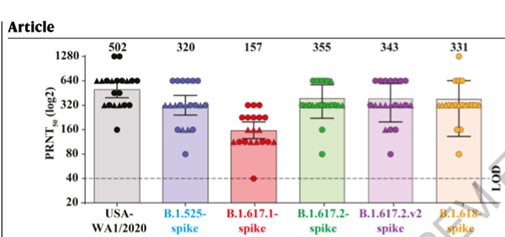
Así, todas las variantes fueron neutralizadas por todos los sueros analizados a títulos de ≥40. Entre las cuatro variantes probadas de origen indio, la B.1.617.1 fue la menos neutralizada, probablemente debido a la presencia de L452R y E484Q, sustituciones en el sitio de unión al receptor que originan resistencia a la neutralización por anticuerpos. Aun así, pese a las reducciones en la neutralización, no se ha demostrado que esto de lugar a la pérdida de la eficacia de la vacuna.
La susceptibilidad de estas variantes recién surgidas a la vacuna BNT162b2 respalda la inmunización masiva como una estrategia central para poner fin a la pandemia de la enfermedad por coronavirus 2019 (COVID-19) en todas las geografías.
Continuarán surgiendo nuevas variantes a medida que persista la pandemia. Hasta la fecha, no hay evidencia de que las variantes del virus hayan escapado de la protección mediada por la vacuna BNT162b2 contra COVID-19. Por consiguiente, aumentar la proporción de la población inmunizada con seguridad y con vacunas autorizadas eficaces sigue siendo una estrategia clave para minimizar la aparición de nuevas variantes y poner fin a la pandemia de COVID-19.
 Newsletter
Newsletter Contacto
Contacto