
Francisco Javier Chorro Gascó
Catedrático de Medicina. Especialista en Cardiología. Profesor Emérito de la Universidad de Valencia. Investigador del Centro de Investigación Biomédica en Red sobre Enfermedades Cardiovasculares (CIBER CV) y del Instituto de Investigación Sanitaria del Hospital Clínico Universitario de Valencia (INCLIVA).
1.- Nuevos enfoques terapéuticos
La insuficiencia cardiaca (IC) es un síndrome clínico originado por causas diversas que conducen a cambios estructurales y funcionales en el corazón, al desarrollo de congestión pulmonar y/o sistémica con importantes limitaciones en la calidad de vida y a una disminución de la supervivencia. Mediante la aplicación de los tratamientos recomendados por las sociedades científicas se consigue mejorar la calidad de vida de estos pacientes, aumentar la tolerancia a los esfuerzos y disminuir la fatigabilidad y los signos y síntomas de congestión. Se evitan hospitalizaciones y mejora el pronóstico; sin embargo, sigue siendo necesario disponer de nuevos tratamientos que superen los resultados actuales. En el ámbito de la investigación traslacional se están desarrollando nuevas aproximaciones en áreas diversas, entre las que se encuentran:
- La regeneración cardíaca para reparar y/o sustituir el miocardio dañado, mejorar la función y atenuar el remodelado adverso (por ejemplo, tras el infarto de miocardio).
- La terapia génica mediante la transferencia de material genético con la ayuda de vectores adecuados para sustituir a genes defectuosos, o mediante la modificación del genoma para disminuir o incrementar una determinada función celular.
- El desarrollo de fármacos dirigidos a nuevas dianas terapéuticas, identificadas gracias al estudio de los mecanismos implicados en el desarrollo de la enfermedad.
1.1.- Medicina regenerativa
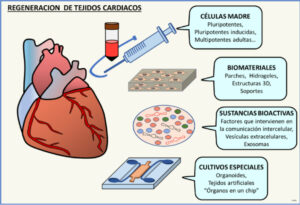
La terapia con células madre o células progenitoras, consiste en la administración de células, con capacidad de diferenciarse en miocitos cardiacos, para sustituir o reparar el tejido dañado. Estas células han de quedar retenidas en el corazón y han de integrarse adecuadamente para mejorar su función. Entre los tipos celulares que se están utilizando se encuentran las células madre pluripotentes obtenidas reprogramando células adultas o las células multipotentes presentes en distintos tejidos (médula ósea, cordón umbilical, tejido adiposo…).
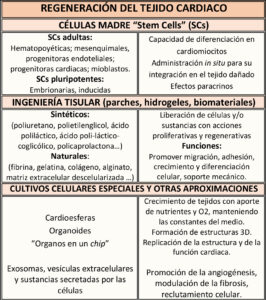
En este ámbito también se están desarrollando biomateriales y tejidos artificiales con fines reparadores, así como tratamientos combinados para favorecer la regeneración cardiaca. Se utilizan parches o hidrogeles inyectables que liberan células, exosomas, material genético o sustancias bioactivas que promueven la migración celular, su adhesión, crecimiento y diferenciación. Pueden actuar sobre la inflamación, la apoptosis, la formación de vasos y de la matriz extracelular o la fibrosis y también pueden mejorar las propiedades mecánicas del corazón.
Forma parte de la investigación sobre la regeneración cardiaca la creación de modelos de organoides, es decir estructuras tridimensionales obtenidas mediante el cultivo de células madre para estudiar la formación de tejidos y/o las acciones de fármacos, así como los “órganos en un chip” en los que los cultivos celulares se desarrollan en microambientes similares a los de los órganos vivos. Entre otros aspectos, se están estudiando los efectos de las sustancias secretadas por estos tipos celulares. Los exosomas derivados de células madre son vesículas extracelulares portadoras de proteínas, lípidos y RNAs, que intervienen en la comunicación entre las células y por lo tanto en los procesos de formación de los tejidos.
En el desarrollo de los procedimientos regenerativos se han de tener en cuenta una serie de consideraciones: seguridad (arritmias, tumores), efectividad a largo plazo, integración en el corazón, coordinación de la actividad eléctrica y mecánica, validación en modelos “in vivo”, escalabilidad, coste-efectividad, irrigación vascular apropiada (nutrición y eliminación de residuos), inmunogenicidad y aspectos éticos y legales.
1.2.- Terapia génica
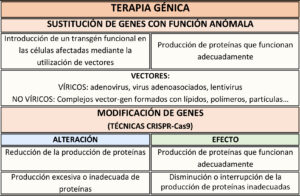
En el ámbito de la IC los objetivos de la terapia génica incluyen, entre otros, la restauración de la función contráctil, la protección celular y la formación de nuevos vasos (angiogénesis). Se utilizan distintas aproximaciones como la sustitución de genes, su edición o su silenciamiento. La transferencia de material genético generalmente se efectúa mediante la utilización de vectores que lo transportan e integran en las células dando lugar, por ejemplo, a la sobreexpresión de sustancias cuya producción está disminuida en las células miocárdicas, como ocurre en determinadas miocardiopatías.
Para mejorar la contractilidad se ha actuado sobre diversos genes con resultados diversos, que requieren replantear las estrategias propuestas y su traslación a la clínica. Entre ellos se encuentran los que intervienen en la síntesis de proteínas implicadas en el proceso de excitación-contracción, como SERCA2a cuya expresión está reducida en la IC. Se están investigando acciones sobre genes que intervienen en las respuestas beta-adrenérgicas, provocando modificaciones en la actividad de distintos receptores. Mediante la sobreexpresión de fosfodiesterasas también se han conseguido resultados favorables en modelos animales de sobrecarga de presión e IC.
Así mismo, se están desarrollando líneas de investigación dirigidas a restablecer la función de canales iónicos transmembrana alterados, con la finalidad de mejorar la contracción y/o evitar el desencadenamiento de arritmias. En la miocardiopatía arritmógena, caracterizada por la aparición de arritmias y el desarrollo de disfunción ventricular, se están estudiando los efectos de actuaciones dirigidas a corregir la codificación anómala de proteínas de las uniones intercelulares.
Las tecnologías de edición de genes (CRISPR: clustered regularly interspaced short palindromic repeats) permiten plantear la modificación de las repercusiones de alteraciones genéticas relacionadas con la IC. Por ejemplo, para bloquear la expresión de Transtiretina con la finalidad de disminuir el depósito y acumulación de sustancia amiloide en el corazón, objetivo que también se persigue mediante el desarrollo de siRNA específicos (RNA pequeño de interferencia). Estas técnicas también permiten plantear la restauración de la funcionalidad de determinados productos genéticos.
También se están estudiando los efectos de la regulación de los procesos implicados en la diferenciación y la reprogramación celular, con la finalidad de inducir o mejorar la formación de nuevos miocitos cardiacos y modular la fibrosis, la hipertrofia y el remodelado adverso.
La investigación en estos ámbitos incluye la evaluación de los objetivos más adecuados, el estudio de la selectividad de sus efectos, la inmunogenicidad, la toxicidad, la formación de tumores y la seguridad, evitando efectos perjudiciales e indeseados.
1.3.- Nuevos fármacos
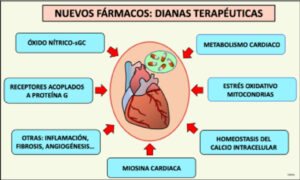
Los avances en el conocimiento de los procesos implicados en el deterioro de la función ventricular promueven el desarrollo de tratamientos dirigidos a dianas concretas, como la producción de las fuentes de energía, la regulación del estrés oxidativo, la inflamación o la fibrosis. El metabolismo inadecuado de los ácidos grasos, la producción ineficiente de la principal fuente de energía (el ATP), o el exceso de formación de sustancias oxidantes repercuten en la función cardiaca. Así, en relación con el metabolismo se investigan los efectos de fármacos que mejoran la eficiencia energética y la contracción y/o la relajación. Entre las vías de actuación se encuentran la reducción del consumo, circulación y oxidación de ácidos grasos o el aumento de la oxidación de la glucosa y los cuerpos cetónicos. Dado el papel de las mitocondrias en la regulación del metabolismo energético y del estrés oxidativo, distintas líneas de investigación van dirigidas a la regulación de su estructura y función.
Otras áreas de estudio están relacionadas con la regulación del calcio intracelular y su interacción con la miosina y otras proteínas implicadas en los procesos de contracción y relajación. Durante la contracción muscular la actina se une a la miosina y la energía química (ATP) se transforma en energía mecánica. Con respecto a la interacción actina-miosina se han desarrollado inhibidores que ya se encuentran en la fase clínica, como el mavacamten, cuya finalidad es controlar estados hipercontráctiles, como ocurre en la miocardiopatía hipertrófica. Por otra parte, con la finalidad de aumentar la fuerza de contracción cuando está disminuida, se han desarrollado fármacos como el omecantiv, que es un activador específico de la miosina, también trasladado a la clínica.
En relación con el factor de crecimiento endotelial, que promueve acciones vasodilatadoras y antifibróticas, se han investigado los efectos de la proteína recombinante serelaxina, aunque los resultados de los ensayos clínicos iniciales han sido neutros en cuanto a la disminución de la mortalidad. Otros fármacos, relacionados con la proteína G, incluyen acciones sobre los receptores de la adenosina, vasopresina, endotelina, o del péptido 1 similar al glucagón, entre otros, con efectos antifibróticos y/o reguladores de la hipertrofia.
También en relación con el óxido nítrico y la estimulación de la guanilato-ciclasa soluble, que tienen efectos vasodilatadores y mejoran la relajación cardiaca, se ha desarrollado el vericiguat, cuya utilización ya se encuentra en la fase clínica. Con respecto a los péptidos natriuréticos se ha desarrollado el ularitide, con efectos diuréticos y vasodilatadores, aunque en los ensayos iniciales no ha disminuido la mortalidad. Otras vías de estudio se relacionan con el control de la inflamación, que se encuentra activada en la IC, o con el control de la fibrosis miocárdica y de la formación de nuevos vasos intramiocárdicos.
En resumen, se dispone de nuevas opciones farmacológicas y a medida que se obtenga o amplie la información sobre sus efectos clínicos se establecerán las recomendaciones para su uso.
Bibliografia: Nuñez J, Chorro FJ, Bodí V, Sanchis J. Insuficiencia Cardiaca. Publicaciones Universitat de València 2020 .- McDonagh TA, et al. Eur Heart J 2023; 44:3627 .- Sapna F et al. Cureus 2023, 15(10): e46486 .- Chowdhury MA et al. Front Physiol 2024;14:1344885 .- Kishino Y et al. J Card Fail 2023; 29:503 .- Ortega M, et al. Int J Mol Sci 2023;24:15698 .- Rios-Navarro C et al. Rev Esp Cardiol 2021; 74:131 .- Hueso L et al. Sci Rep 2017;7:9962 .- Correale M et al. Front Cardiovasc Med 2023; 10:1157472 .- Argirò A et al. Rev Esp Cardiol. 2023;76:1042 .- Kalinski JK et al. Am J Card Drugs 2024; 24:591 .- Haryani A et al. Cureus 2024; 16(3): e57180 .- Zhang Z et al. Biomed Pharmacother 2024 Apr:173:116413 .- Alfieri M et al. J Cardiovasc. Dev Dis. 2024; 11, 125.
Dejar Comentario
 Newsletter
Newsletter Contacto
Contacto





